Após mais de duas décadas sem avanços significativos, dois medicamentos inéditos chegam ao Brasil com resultados comprovados, e mudam a forma de encarar a doença que afeta mais de 57 milhões de pessoas no mundo.
Por Juba Paixão
Por décadas, o diagnóstico de Alzheimer foi seguido de uma sentença quase invariável: nenhum tratamento seria capaz de alterar o curso da doença. Os medicamentos disponíveis, os mesmos há mais de vinte anos, podiam aliviar sintomas, mas não freavam o avanço da destruição neurológica. Isso começou a mudar.
Dois anticorpos monoclonais, o lecanemabe e o donanemabe, chegaram ao Brasil com aprovação da Anvisa e resultados clínicos publicados nas principais revistas científicas do mundo. Não são uma cura, mas representam, pela primeira vez, medicamentos com capacidade comprovada de modificar a trajetória da doença, e não apenas de mascarar seus efeitos.
Como funcionam
O Alzheimer tem como uma de suas marcas a formação de placas de proteína beta-amiloide no cérebro, que se acumulam ao longo de anos antes mesmo dos primeiros sintomas aparecerem. Tanto o lecanemabe quanto o donanemabe atuam como anticorpos que se ligam a esses aglomerados e os removem, atacando a doença em sua origem biológica, não apenas em suas consequências cognitivas.
O lecanemabe tem afinidade especial pelas chamadas protofibrinas solúveis, consideradas as formas mais tóxicas e precoces do acúmulo amiloide. O donanemabe atua com foco nas placas já formadas, em estágio mais avançado de insolubilização. Mecanismos distintos, mesma direção: remover o que não deveria estar lá.
São as primeiras drogas aprovadas depois de mais de 20 anos que realmente modificam a evolução da doença — e não apenas tratam os sintomas”, destaca Claudia Suemoto, professora associada de Geriatria da FMUSP e coordenadora do Banco de Encéfalos da USP.
O lecanemabe foi avaliado no estudo CLARITY-AD, um ensaio clínico de fase 3, multicêntrico, duplo-cego e controlado por placebo, que reuniu 1.795 participantes com comprometimento cognitivo leve ou demência leve por Alzheimer, com acúmulo confirmado de amiloide no cérebro.
O estudo envolveu pacientes dos Estados Unidos, Austrália, Canadá, China, países europeus e Japão, e demonstrou uma redução de 27% no declínio cognitivo ao longo de 18 meses em comparação ao placebo. Dados de extensão do estudo, acompanhando pacientes por 36 meses, confirmaram benefícios contínuos.
O donanemabe foi avaliado no estudo TRAILBLAZER-ALZ 2, com 1.736 participantes em fase inicial da doença. Os resultados também demonstraram retardo estatisticamente significativo da progressão cognitiva e funcional, com substancial remoção das placas amiloides. Ambos os estudos foram publicados no The New England Journal of Medicine, a revista médica de maior prestígio científico do mundo.
Serve como prevenção?
Esta é uma das fronteiras mais promissoras da pesquisa atual, e a resposta ainda está em construção pela ciência. O que se sabe é que os medicamentos, em sua aprovação atual, são indicados para pessoas que já apresentam sintomas iniciais confirmados. Mas a hipótese de que agir antes do aparecimento dos sintomas poderia ser ainda mais eficaz. No momento está em fase de testes com rigor.
O estudo AHEAD 3-45, conduzido pela Eisai com financiamento do National Institute on Aging dos Estados Unidos, é o maior ensaio de prevenção do Alzheimer já realizado. Ele testa o lecanemabe em pessoas cognitivamente saudáveis, entre 55 e 80 anos, que já apresentam acúmulo intermediário ou elevado de amiloide no cérebro, identificado por exame de imagem, mas ainda sem nenhum sintoma. O estudo, de fase 3, tem duração de 216 semanas e está totalmente recrutado, com resultados esperados nos próximos anos.
A lógica é poderosa: se o amiloide começa a se acumular décadas antes dos primeiros sinais clínicos, intervir nessa janela silenciosa pode mudar completamente o prognóstico.
Os dados dos ensaios já realizados reforçam esse raciocínio, os pacientes que responderam melhor ao tratamento foram justamente aqueles tratados nos estágios mais precoces da doença. Ainda não é prevenção confirmada, mas a ciência está claramente apontando nessa direção.
Os dados dos ensaios clínicos mostram que o tratamento é mais eficaz quanto mais cedo é iniciado, o que coloca o diagnóstico precoce como prioridade absoluta” declara o Alzheimer’s Disease International (ADI).
As instituições e as equipes por trás da pesquisa
O lecanemabe é desenvolvido pela farmacêutica japonesa Eisai, que lidera a pesquisa e as submissões regulatórias globais, em parceria comercial com a americana Biogen. A pesquisa básica contou com a participação de cientistas da Universidade de Washington, da Universidade de Yale e do próprio Eisai Research Institute. O donanemabe é produzido pela Eli Lilly, com sede em Indianápolis, Estados Unidos. Todos os estudos foram conduzidos com supervisão de comitês independentes de segurança e revisão por pares nas mais exigentes publicações científicas internacionais.
No Brasil
O donanemabe, comercializado como Kisunla, foi aprovado pela Anvisa em 24 de abril de 2025, o primeiro da nova classe a chegar ao Brasil. O lecanemabe, vendido como Leqembi, recebeu aprovação da Anvisa em 22 de dezembro de 2025, com chegada ao mercado prevista para o fim de junho de 2026, após a definição de preço junto à CMED. O Brasil torna-se assim o primeiro país da América Latina a contar com duas terapias modificadoras do Alzheimer aprovadas em sequência.
Os benefícios clínicos, embora estatisticamente significativos, são considerados modestos por parte dos especialistas, e a durabilidade dos efeitos em longo prazo ainda está sendo acompanhada. Ambos os medicamentos podem causar anomalias de imagem relacionadas à amiloide, conhecidas como ARIA, que incluem microhemorragias e inchaços cerebrais, o que exige monitoramento rigoroso por ressonância magnética nos primeiros meses de tratamento. O custo elevado também representa um desafio real de acesso, e a incorporação ao SUS não está prevista no curto prazo.
Histórico
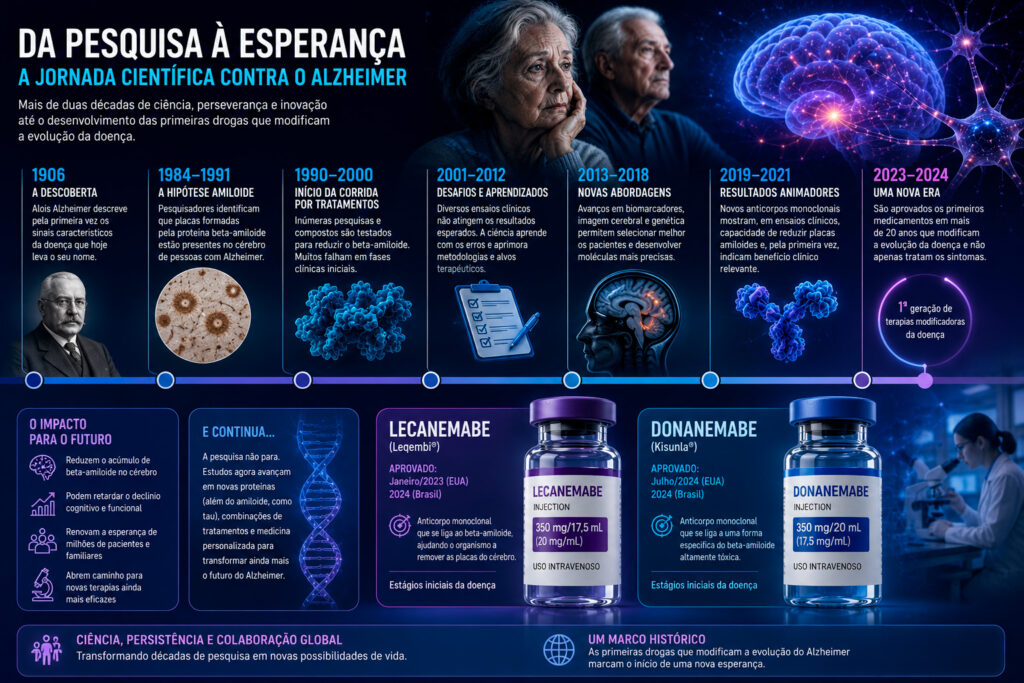
A linha do tempo da evolução científica no combate ao Alzheimer, destaca como décadas de pesquisa, erros, descobertas e avanços tecnológicos culminaram no surgimento dos primeiros medicamentos capazes de modificar a progressão da doença, e não apenas aliviar sintomas.
A cronologia começa em 1906, quando o médico alemão Alois Alzheimer descreveu pela primeira vez os sinais da enfermidade que posteriormente receberia seu nome. Esse marco inaugura mais de um século de estudos sobre o funcionamento do cérebro e os mecanismos da neurodegeneração.
Entre as décadas de 1980 e 1990, ganha força a chamada “hipótese amiloide”, teoria que associa o Alzheimer ao acúmulo da proteína beta-amiloide no cérebro. A partir daí, a comunidade científica inicia uma intensa corrida global em busca de tratamentos capazes de interferir diretamente nesse processo biológico.
Nos anos 1990 e 2000, a pesquisa entra em uma fase de grande expansão. Diversos compostos e terapias experimentais começam a ser testados, mas muitos falham nas etapas clínicas. Apesar das frustrações, esse período foi essencial para o amadurecimento das metodologias científicas e para a compreensão mais profunda da doença.
Entre 2001 e 2012, a ciência enfrenta desafios importantes. Muitos estudos não alcançam os resultados esperados, o que fez pesquisadores a rever estratégias, aprimorar biomarcadores e investir em tecnologias mais precisas de diagnóstico e monitoramento cerebral.
A partir de 2013, novas abordagens científicas e avanços em neuroimagem, genética e biotecnologia permitem selecionar melhor os pacientes e desenvolver moléculas mais direcionadas. Esse refinamento aumenta a precisão das pesquisas e abre caminho para resultados mais promissores.
Entre 2019 e 2021, começam a surgir evidências concretas de que anticorpos monoclonais poderiam reduzir as placas beta-amiloides no cérebro e retardar o declínio cognitivo em alguns pacientes. Pela primeira vez em décadas, a comunidade científica passa a enxergar a possibilidade real de alterar a evolução da doença.
A linha do tempo culmina em 2023 e 2024, com a aprovação dos medicamentos Lecanemabe e Donanemabe, considerados um marco histórico na neurologia moderna. Embora não representem a cura do Alzheimer, essas terapias inauguram uma nova era ao atuarem diretamente nos mecanismos biológicos da doença.
A atual fase da pesquisa reforça os impactos esperados para o futuro: retardar o avanço da doença, ampliar a qualidade de vida dos pacientes, gerar novas possibilidades terapêuticas e estimular o desenvolvimento de tratamentos ainda mais eficazes.
Fontes:
Anvisa — Aprovação do lecanemabe (Leqembi): gov.br/anvisa — jan. 2026
Anvisa — Aprovação do donanemabe (Kisunla): Agência Brasil — abr. 2025
Van Dyck, C. H. et al. Lecanemab in Early Alzheimer’s Disease. New England Journal of Medicine, v. 388, n. 1, p. 9–21, 2023
Ensaio CLARITY-AD — ClinicalTrials.gov: NCT03887455
Ensaio TRAILBLAZER-ALZ 2 — Eli Lilly / NEJM, 2023
Estudo AHEAD 3-45 (prevenção) — ClinicalTrials.gov: NCT04468659 — Eisai / National Institute on Aging
Eisai / Biogen — Comunicado oficial CLARITY-AD: alzheimer-europe.org, set. 2022
Alzheimer’s Disease International (ADI): alzint.org
SanarMed — “Lecanemabe chega ao Brasil em 2026”: sanarmed.com, fev. 2026
CNN Brasil — “Novo medicamento para Alzheimer aprovado nos EUA”: cnnbrasil.com.br, jul. 2024
Gov.br/Ebserh — HUCAM-UFES: entrevista com Dr. Roni Mukamal sobre Alzheimer, set. 2023 e out. 2025











